上市後臨床追蹤
由於高風險/創新醫療器材的上市前臨床資料較為侷限,主管機關會條件性核發醫材許可證,並要求廠商進行上市後臨床追蹤。
關於以下類型的醫療器材會被強制要求進行上市後臨床追蹤:
• 創新之醫療器材;
• 高風險之醫療器材;
• 由於其安全性或性能等出現新資訊而受到影響的醫療器械;
我們擁有豐富的上市後臨床追蹤的經驗,與製造商、代理商、醫療院所及主管機關密切配合,近年來我們服務產品囊括玻尿酸皮下植入劑、質子治療系統、腹主動脈血管支架等多領域高風險醫材。
我們可提供上市後臨床追蹤的服務,依照您的產品擬定上市後臨床追蹤計畫,並協助您收集上市後臨床資料。
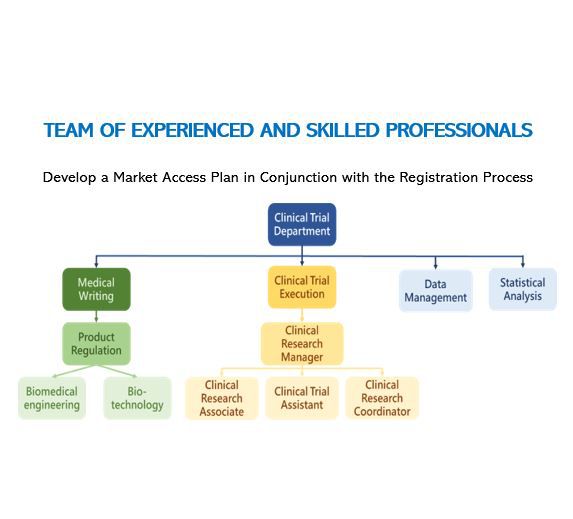
臨床評價報告
醫療器械臨床評價是指註冊申請人透過臨床前測試報告、體外動物實驗結果臨床文獻資料、臨床經驗資料、臨床試驗等資訊對註冊產品及已上市產品做技術、生物、及臨床各方面的比較,確認註冊產品及已上市產品於使用要求或者適用範圍等方面之相似度,並進行註冊產品之有效性及安全性之評估。
我們依您的需求提供歐盟、中國、新加坡等地區的臨床評估報告撰寫服務。
服務內容如下:
• 類似品對比搜索
• 國內外各大資料庫文獻搜索
• 國內外上市後不良事件各大資料庫搜索
• 臨床文獻與非臨床類資料整合
• 撰寫臨床評估報告

臨床試驗
指在符合優良臨床試驗規範認定的醫療器材臨床試驗機構中,對擬申請上市註冊的醫療器材,於正常使用條件下的安全性和有效性進行確認/驗證的過程。當地衛生主管機關會要求高風險或創新醫療器材進行臨床試驗。
我們依您的需求提供以下服務:
• 臨床試驗規劃
• 衛生主管機關審查送件
• 人體試驗委員會審查送件
• 臨床試驗執行
• 臨床試驗現場專業人員委派(CRC/CRA)
• 臨床試驗資料處理、生物統計分析
• 臨床試驗報告撰寫等
理工優勢
我們擁有案件管理系統
嚴守服務品質
我們在多國建立QT團隊
提供多元服務
我們提供豐富訓練與考核
培養專業人才
我們透過Cookies蒐集您的瀏覽記錄,以了解您如何使用我們的網站,從而分析及改善您的體驗。如繼續使用我們的網站,即表示您接受我們使用 Cookies。